James Coleman
プロテイン の 代わり に なる もの 縫い 仕組み6/5/2018 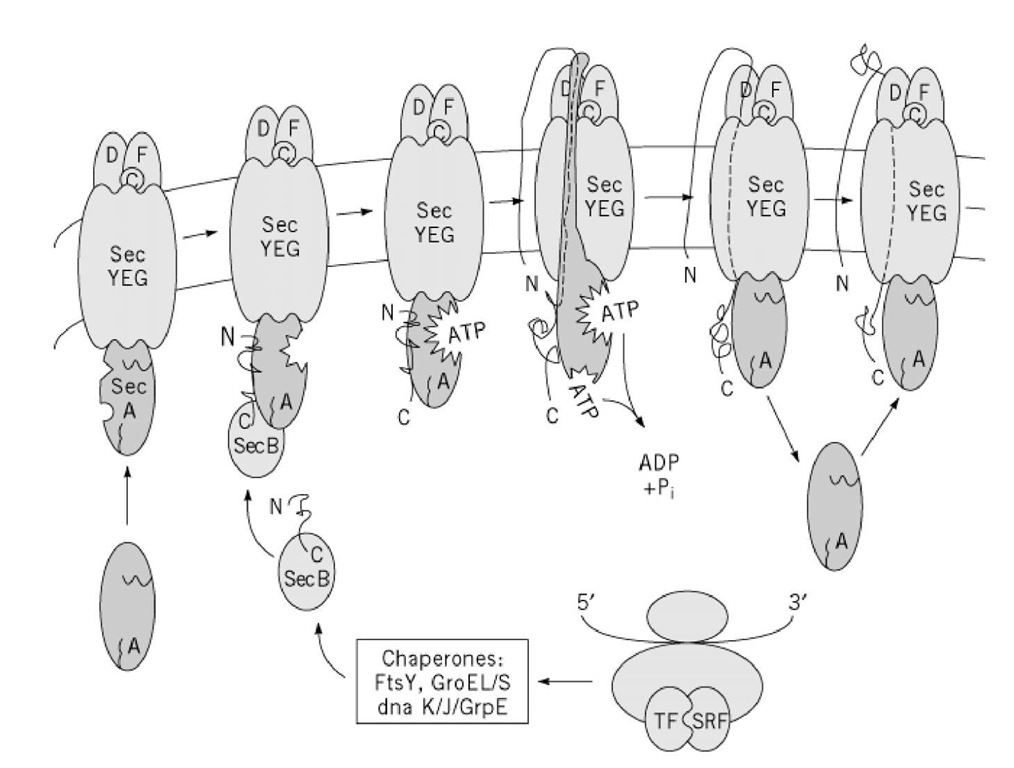 細胞によって作られたタンパク質の大部分は、細胞内に保持される。特別なサブセットのみが細胞外に分泌される. 細胞によって分泌されるタンパク質は、他の細胞へのシグナル伝達、細胞を取り囲む不溶性細胞外マトリックスの形成、および細胞外物質の分解を含むいくつかの主要な機能を有する. 分子生物学は、新たに合成されたタンパク質が、原形質膜の疎水性障壁を通じた分泌および輸送のためにどのように選択されるのかを説明するのに役立っている(Protein biosynthesis参照). 細胞によって作られたタンパク質の大部分は、細胞内に保持される。特別なサブセットのみが細胞外に分泌される. 細胞によって分泌されるタンパク質は、他の細胞へのシグナル伝達、細胞を取り囲む不溶性細胞外マトリックスの形成、および細胞外物質の分解を含むいくつかの主要な機能を有する. 分子生物学は、新たに合成されたタンパク質が、原形質膜の疎水性障壁を通じた分泌および輸送のためにどのように選択されるのかを説明するのに役立っている(Protein biosynthesis参照).
プロテイン の 代わり に なる もの 縫い 仕組み クチコミ新たに合成されたタンパク質を輸送するための機構は、細菌から哺乳類に高度に保存されている. しかし、重要な違いは、バクテリアは細胞膜を横切って外界にタンパク質を直接移動させるのに対し、真核細胞はそれらを特殊な細胞内小器官である小胞体. 新たに合成されたタンパク質は、小胞体から一連の担体小胞を介して細胞表面に運ばれる. したがって、原核および真核タンパク質分泌を別々に考慮することが有用である. 1. 細菌からのタンパク質の輸出 細菌は、細胞生物学的観点から極めて単純である. グラム陽性細菌は、細胞膜を外界から分離している膜のみを有する.プロテイン の 代わり に なる もの 縫い 仕組み ミュゼグラム陰性細菌は、ペリプラズム空間によって内膜から分離された第二の外膜を有する. この場合、輸出される新たに合成されたタンパク質は、内部原形質膜に加えて外膜をも横切らなければならない. 膜を横切る転位の基本的要素は普遍的であるようである(1). 折り畳まれていないタンパク質が通過することができる小さな細孔または穴が膜を横切る.プロテイン の 代わり に なる もの 縫い 仕組み 本開かれたタンパク質を穴を通して押し出すためにエネルギーが使用される. 分子シャペロンタンパク質は、細孔の細胞質側に存在し、タンパク質を折り畳まれていない状態に維持し、細孔を貫通している.プロテイン の 代わり に なる もの 縫い 仕組み 楽天シャペロンは、輸出されるタンパク質が、シグナル配列、通常、タンパク質のアミノ末端にある隣接するアミノ酸の領域を有するため、細胞質タンパク質から輸出されるタンパク質を区別する. タンパク質が膜を横切ると、追加のシャペロンは正しいタンパク質の折りたたみを促進することができる. 細菌によるタンパク質の輸出に関する研究の多くは、グラム陰性菌である大腸菌(Escherichia coli)を利用している.プロテイン の 代わり に なる もの 縫い 仕組み ないE. 少なくとも2つの異なるATP駆動輸送系があり、1つはsec A系(Sec変異体/タンパク質参照)を使用してペリプラズム空間にタンパク質をポンプ輸送するシステム(2)であり、もう1つはABC - 結合カセット)ファミリーのタンパク質をE. 同時に大腸菌膜(3). 1. 1. タンパク質輸送のsecAシステム E. 大腸菌(coli)は、輸出を目的とするタンパク質を産生するが、シグナル配列を含むプレタンパク質として作製される(4). 大部分のタンパク質では、これらのシグナル配列は、タンパク質のアミノ末端で、正に荷電したアミノ末端、少なくとも6つの連続した疎水性アミノ酸、およびシグナル後にシグナルを除去するシグナルペプチダーゼの切断部位を有する一連の連続したアミノ酸である転座. 新たに合成されたタンパク質中のシグナル配列の存在は、タンパク質シャペロンをそれに結合させ、その折りたたみを遅らせる.プロテイン の 代わり に なる もの 縫い 仕組み ないE中に少なくとも2つの主要なシャペロン系があるようである. 大腸菌. 1つは、シグナル配列を含む新たに合成されたタンパク質に結合する四量体のサイトゾルタンパク質secBを含む. これは、新たに合成されたポリペプチド鎖の全長に亘って結合し、その天然の立体配座を取らないようにする(2). シャペロンの異なるクラスは、分泌タンパク質がリボソーム上で合成されているときに新生鎖に結合する. そのようなシャペロンの例は、リボ核タンパク質、シグナル認識タンパク質(SRP). E. coli SRPは、4つの. 5 S RNA分子および単一のタンパク質、GTPアーゼであるFfh;すなわち、それはグアノシン三リン酸を加水分解する(5).プロテイン の 代わり に なる もの 縫い 仕組み 読み折り畳まれないように保つシャペロンと複合体を形成した輸出向けのタンパク質は、バクテリア原形質膜上の受容体と相互作用して、膜を横切る移行を開始する. secB受容体はsecAであり、SRP受容体は別のGTPaseであり、FTsY(5). 従って、シグナル配列は2つの機能を有する:(1)シャペロンを引き付けること、および(2)複合体を細胞膜受容体に標的化することを助けること. 実際の転座事象は、膜貫通孔. E. 大腸菌は、いくつかの付属タンパク質を含む3つの主要な膜タンパク質(secY、secE、およびsecG)からなる秒YEG複合体からなる.プロテイン の 代わり に なる もの 縫い 仕組み ワイヤー2番目のYEG複合体は、折り畳まれていないタンパク質が細胞外に出て行く間隙を形成する. 転位は、ミシン針またはピストン(6)に類似した機構によって、折り畳まれていないペプチドを孔を通して押し出すことを含み、. 末梢膜タンパク質(secA)は、アミノ末端シグナルペプチドおよび隣接するアミノ酸によって形成される25残基のループをとり、ループを膜に押し込む. アミノ末端アミノ酸は細胞質に残っている. これを行うために、secAタンパク質は、secAタンパク質のアームを一時的に膜を横切って部分的に挿入させる顕著なATP駆動の立体配座変化を経る.プロテイン の 代わり に なる もの 縫い 仕組み 子供プッシング工程の後、ATPは加水分解され、secAは細胞質の場所に戻され、第2の転位ポンピングサイクルの準備が整う. シグナルペプチドは、ペリプラズム空間に位置する「シグナルペプチダーゼ」によって切断される. 25残基の段階でのさらなるトランスロケーションは、タンパク質活性のさらなるサイクルによって推進され得る. しかし、最初の段階の後に、膜貫通陽子原動力によって、さらなる転座が促進される(図2C)。. 1). 図1. タンパク質輸送のSecAシステム. シャペロンは新生タンパク質に結合して、それを膜上の受容体SecAに広げないようにする.プロテイン の 代わり に なる もの 縫い 仕組み ルータSecAは、タンパク質細孔を介して膜を横切ってタンパク質を転位させる(SecY1立体配座変化. 細菌は、それを引くのではなく、転座チャネルを横切ってタンパク質を押すことができる。なぜなら、エネルギー源ATPは専ら細胞質であるからである. ペリプラズム空間に入ると、分泌されたタンパク質はジスルフィド結合を形成し、プロテイナーゼ耐性コンフォメーションに折り畳まれる. このような折りたたみは、タンパク質が外膜にはほとんど記載されていない穴を通って輸送される前に必要である. 1. 2. ABCタンパク質媒介輸出 輸出向けのいくつかのタンパク質はEの細胞質で認識される. 完全に異なるクラスのシグナル配列による大腸菌.プロテイン の 代わり に なる もの 縫い 仕組み ランキングこれらの場合、配列はC末端にあり、輸送後シグナルペプチダーゼによって切断されない. このタイプのシグナル配列を有するタンパク質は互いに密接に関連しており、毒素、プロテイナーゼ、およびリパーゼなどのタンパク質を含む. シグナル配列は、ATP結合カセット(ABC)ファミリーのATP駆動タンパク質トランスロケーター(3,7)の異なるクラスの原形質膜タンパク質によって認識される. ABCタンパク質は、2つの細胞質ATP結合ドメインおよび2つの疎水性ドメインを有し、6つの膜貫通配列. それらは、単一のポリペプチドのいずれかであってもよく、またはいくつかのポリペプチド. 細菌ABCの輸出と2つのアクセサリータンパク質との複合体は、内部および外部の細菌膜の両方を横切って同時に細胞質タンパク質を輸出することを可能にする.プロテイン の 代わり に なる もの 縫い 仕組み ネットワーク輸送複合体のアセンブリは、基質結合(8)によって誘発され、. 2. 真核生物からのタンパク質の輸出 細菌とは異なり、真核細胞は細胞内膜. これらの膜のかなりの部分がタンパク質の輸出に関与している. したがって、真核生物におけるタンパク質の輸送は、膜を横切る移行を含むが、細胞内区画を通じた新たに合成されたタンパク質の輸送も含む(9). したがって、真核生物におけるタンパク質の輸出は、細菌よりもはるかに複雑なプロセスである.プロテイン の 代わり に なる もの 縫い 仕組み ワイヤー新しく合成されたタンパク質が真核細胞表面に達する前に細胞内経路を知ることが必要になります(タンパク質標的も参照). 2. 1. 輸出されたタンパク質の細胞内トラフィッキング 大部分の場合、真核生物は原形質膜を越えてタンパク質を直接分泌しない. 代わりに、新たに合成されたタンパク質は、細胞質から細胞内小器官に転位し、小胞体(ER). ERは、細胞質全体に広がり、核膜と連続する一連の膜状の槽と細管である. 我々が見るように、ER膜および細菌膜を横切ってタンパク質を移動させるための機構は、膜貫通細孔. なぜERを持っているのですか? ERの進化上の利点に関する共通の推測は、それが、細胞外の世界の厳しさにさらされることなく、輸出されたタンパク質が折りたたまれオリゴマー化することができる制御された環境を提供することである.プロテイン の 代わり に なる もの 縫い 仕組み 本これに関して、ERの内腔は、グラム陰性細菌におけるペリプラズム空間に似ている. ERで正しく折りたたまれてオリゴマー化されたタンパク質は、細胞の外側に輸送されなければならない. ERからの輸送の初期段階は、輸出されたタンパク質を貨物として含む小膜ベシクル(通常は担体小胞と呼ばれる)の形成である(10,11). 担体小胞の形成は移行帯(transitional zone)と呼ばれる特別なER領域で起こり、ベシクル膜に曲率を与え、ドナーERからそれを挟み込むために細胞質コートを必要とする(12).プロテイン の 代わり に なる もの 縫い 仕組み ランキング担体小胞が形成された後、それはその標的を認識して融合しなければならない. 小胞(v-SNARE)および標的膜(t-SNARE)上のタンパク質(13)は、認識および融合(エキソサイトーシス参照). 担体小胞がERを離れるとき、それは原形質膜に直接は向かわず、オルガネラと融合するが、真核生物の分泌経路上の必須の方法であるゴルジ複合体. ゴルジ複合体は膜状槽のスタックであり、形態学的にはパンケーキのスタックと類似している. 担体小胞は、ゴルジ体スタックのシス末端に入り、トランス側から出る. 輸出されるタンパク質は、セリン、トレオニン(O-グリコシル化)またはアスパラギン残基(N-グリコシル化)に結合したオリゴ糖鎖に6または9炭素糖を付加または除去する一連のグリコシル化工程を経る.プロテイン の 代わり に なる もの 縫い 仕組み ナイ添加された糖は、細胞外の世界に分泌された後、輸出されたタンパク質をしばしば迅速なタンパク質分解から保護することができる. 固有のクラスのオリゴ糖が、新たに合成されたリソソーム酵素に添加され、それにより、それらが一次リソソームへの分泌経路から逸脱することを可能にする. 第2の発芽事象は、ゴルジ複合体のトランス領域から起こる. 第2のコーティング機構は、輸出のためのグリコシル化タンパク質を含有する分泌小胞の形成を引き起こす. ポストゴルジ体分泌小胞は、拡散または微小管に沿った輸送のいずれかによって原形質膜に移動する. 分泌小胞が原形質膜に到達すると、それらの膜および原形質膜が融合して1つの連続二重層を形成し、エキソサイトーシスとして知られるプロセス.プロテイン の 代わり に なる もの 縫い 仕組み クチコミ融合工程は、輸出されたタンパク質の細胞外培地への放出をもたらす(図1C)。. 2). 図2. 真核生物の分泌経路. 分泌タンパク質は、(a)細胞質から小胞体(ER)への転位によって膜輸送系に入る(b)ERにおいて、タンパク質はERからゴルジ複合体(GC)担体小胞にパッケージングされ、 GC. タンパク質がGCを通って進むにつれて、(d)グリコシル化される.プロテイン の 代わり に なる もの 縫い 仕組み ナイ(e)が/トランスゴルジネットワーク(TGN)に達すると、それらは(g)タンパク質が原形質膜(PM)に輸送される分泌小胞に分類され、. 細胞表面で分泌タンパク質は、(h)細胞外環境に放出される. タンパク質の輸出または分泌のこの経路は、酵母、原生動物、および筋肉細胞および線維芽細胞などの哺乳動物細胞を含む、ほとんどの生物に従うものである. それは、内分泌細胞および外分泌細胞などの特殊な細胞、および好中球または細胞傷害性Tリンパ球などの造血系の細胞に見られる特殊な経路と区別するために、構成的経路と一般に呼ばれています .プロテイン の 代わり に なる もの 縫い 仕組み クチコミこのような細胞では、新たに合成されたタンパク質は正常な生合成経路から流出し、分泌顆粒に貯蔵される(14). 分泌顆粒と原形質膜との融合は、通常、外部刺激によって引き起こされる. このクラスの分泌タンパク質の輸出は刺激によって制御されるため、貯蔵経路からのタンパク質の放出を制御することが規制放出と呼ばれている. 真核生物のタンパク質輸送経路は高度に保存されている.プロテイン の 代わり に なる もの 縫い 仕組み ルーター原虫、酵母および哺乳動物細胞は、タンパク質をERに転位させ、グリコシル化し、ゴルジでそれらを選別し、それらをエキソサイトーシスによって原形質膜を越えて輸送するために、. 2. 2. ER膜を通過するトランスロケーション ER膜を横切って新たに合成されたタンパク質の転位は、細菌の原形質膜タンパク質を横切る転位と多くの類似点を示す(1,15,16).プロテイン の 代わり に なる もの 縫い 仕組み 子供タンパク質は細胞質内で折りたたまれない. それらは、トランスコーン、secY、E、およびG遺伝子によって作製された細菌タンパク質に非常に類似した3つのサブユニットを有するトランスロンコを介して、原形質膜を介して供給される. 電子顕微鏡法により、これらの細孔は直径が約8〜10nmであり、中心細孔が2nmであり、1の伸長された水和ペプチドの通過を可能にするのに十分である. 直径1nm. これらの孔は今や認識されることができる(17). 酵母では、タンパク質は2つの異なるタイプのトランスロケーション機構によってERの孔を横切る. 一つは、合成が完了したタンパク質を転位させるATP駆動プロセスである.プロテイン の 代わり に なる もの 縫い 仕組み 子供翻訳プロセスへの他のカップルの翻訳. この輸送様式では、リボソームは、タンパク質性の輸送細孔であるトランスロコーンに結合し、それが合成されている間に新生の列を細孔を通して供給する. 哺乳動物細胞は、トランスロケーションの共翻訳のみを有する. トランスロケーションが同時翻訳である場合、新生鎖はシグナル認識粒子によって細胞質で認識され、リボソーム、新生鎖およびシグナル認識粒子の複合体が小胞体に到達するまでタンパク質合成をさらに停止させる. 3). 図3. ER膜を横切る移行. (a)シグナル認識粒子(SRP)は、新生タンパク質上のシグナル配列に結合し、リボソームによるタンパク質の合成を停止する.プロテイン の 代わり に なる もの 縫い 仕組み ネット(b)SRPは、その受容体に結合することにより、タンパク質およびリボソームをER膜上のトランスコノンにもたらす. (c)リボソームが正しく配置され、タンパク質がトランスロコンに挿入されたときにタンパク質合成が再開する. (d)タンパク質は、ERの内腔に完全に転位して分泌タンパク質になるか、または膜を部分的に転位して一体化した膜タンパク質になる. 新生鎖は細胞質に入るので、適切なアスパラギン残基上でグリコシル化され、ジスルフィド結合を形成する.プロテイン の 代わり に なる もの 縫い 仕組み ルータ折りたたみは、BiP、カルネキシン、ペプチジルプロリルシス/トランスイソメラーゼ、およびタンパク質ジスルフィドイソメラーゼ(18)などのアクセサリータンパク質との関連によって完了する. タンパク質はまたERの内腔でオリゴマー化する. 例えば、プロトコル標識は、ヒドロキシプロリンとヒドロキシリシン残基との間の架橋を伴う拡張されたコイルドコイル構造で三量体化する(ヒドロキシル化(リジン、プロリン)参照). コラーゲンプロトフィブリルの架橋が阻害されると、不適切に折り畳まれたコラーゲンはERを離れることができず、迅速に分解される. 分泌されたタンパク質であるα1-アンチトリプシン.プロテイン の 代わり に なる もの 縫い 仕組み 楽天疾患では、α-アンチトリプシン欠損、タンパク質の突然変異が正しい折りたたみを妨げる可能性があります. これらの2つの例は、ERを離れるタンパク質を調査し、不適切に折りたたまれたタンパク質の輸出を防ぐ品質管理システムが存在することを示している. 最近のデータは、不適切に折り畳まれたERタンパク質がERから細胞質へと戻され、プロテアソームによって分解されることを示唆している(19). 2. 3. ERから分泌タンパク質のトラフィック ERから正確に折りたたまれオリゴマー化されたタンパク質を得るために、小胞は移行要素中に形成され、輸出されるタンパク質を含むが、BiLP(20)などのER内腔の常在タンパク質は除外する.プロテイン の 代わり に なる もの 縫い 仕組み 読み小胞を形成させるコートは現在、COPII. 酵母COPIIには、sec31p、sec13p、sec23p、およびsec24pの4つのサブユニットが含まれている(sec変異体参照). COPIIコートを組み立てるには、ER膜(12)に小さなGTPアーゼSar1とグアニンヌクレオチド交換因子Sec12pが必要である. 4). コートされた小胞はゴルジを離れてv-SNARE分子(エキソサイトーシス参照)の補体を持ち、シス - ゴルジネットワークと融合する.プロテイン の 代わり に なる もの 縫い 仕組み ルーター酵母では、これらはSec22p、Bos1p、およびBet1pである. BiPのような常在性タンパク質は、小さいベシクルに入るには大きすぎる複合体にオリゴマー化されているので、コーティングされた小胞の内腔から除外され得る. ある程度、輸出されたタンパク質は、保持シグナルがなくERで保持されないタンパク質である. 分泌されたタンパク質の輸出は、他の場所に行くための情報がないため、デフォルトで行われるだろう.プロテイン の 代わり に なる もの 縫い 仕組み ネットワークしかし、陽性選別が起こるという証拠がある(21). 5). 酵母では、分泌されたタンパク質インベルターゼは、ゴルジへの輸送に必要とされる膜結合ERタンパク質(Emp24p)によって認識される(22). さらに、貨物タンパク質はERを離れるにつれて濃縮される(23,24). ER内腔の大部分の可溶性常在タンパク質はグリコシル化されていないので、輸出されたタンパク質はレクチンによって認識され、レクチンはそれらを出芽小胞に集中させる. タンパク質ERGIC-53は、ERとゴルジの間を再循環し、新たに合成された分泌タンパク質に見出されるマンノース残基に結合する能力を有するレクチンである(25).プロテイン の 代わり に なる もの 縫い 仕組み ナイERGIC-53のようなタンパク質は分泌タンパク質に結合し、マンノースリン酸受容体が新しく形成されたリソソーム酵素をプレリソソームコンパートメントに運ぶのと同じようにゴルジ複合体に積極的に運ぶ. 図4. ERからGC担体小胞の形成. ER〜GC担体小胞は、COPIIコート(Sar1、Sec13 / 31pおよびSec23 / 24p)で形成され、. 成分は、(a)GTPase Sar1(そのGTP状態)、v-SNAREおよびカーゴ分子に結合する. (b)Sec13 / 31pがSar1に結合し、次に(c)Sec23 / 24pが複合体全体に結合する. 未知の機構により、COPIIコート(d)は小胞をER膜から芽出しさせ、そして(e)被覆を外して成熟担体小胞に導き、ゴルジ複合体と融合する.プロテイン の 代わり に なる もの 縫い 仕組み 楽天他のタイプの小胞の形成は、異なるコーティングタンパク質を用いて同様の工程を含む可能性がある. 図5. ERとGCの間のタンパク質のソーティング. (a)GCへの担体小胞融合に必要な分泌用の貨物タンパク質およびv-SNAREを、ER常在タンパク質からCOPII被覆小胞に選別する. GCへの送達後、貨物タンパク質は分泌経路を通って継続する.プロテイン の 代わり に なる もの 縫い 仕組み ナイ(b)しかしながら、ERからGCへのトラフィッキング工程に必要なv-SNARESおよびGCに誤って輸送されたER常在タンパク質は、逆行性輸送を介してCOPI被覆担体小胞によるERへ戻ることができる. おそらく担体タンパク質であるERGIC-53は、ERとGCとの間を循環し、ERに保持されるタンパク質から分泌タンパク質を選別するのを助けることができる.プロテイン の 代わり に なる もの 縫い 仕組み ランキングERGIC-53およびv-SNAREタンパク質などのタンパク質は、ゴルジ体からERにリサイクルすることができます. ゴルジからER流への小胞は、COPIコモマーと呼ばれるコモマーから構成されています. コモマーは7つのサブユニット. コートマーコート形成中の小さなGTPase活性は、ADPリボシル化因子(ARF1)であり、. ER由来キャリア小胞とゴルジ膜との融合は、小胞膜のv-SNARE Sec22p、Bos1p、およびBet1p、および小胞膜のsed-Golgi t-SNARE、sed5タンパク質. さらに、ラビファミリーのメンバーである第2のクラスの小さなGTPアーゼが必要とされている(26).プロテイン の 代わり に なる もの 縫い 仕組み こどもrab GTPアーゼは、あるオルガネラに特異的なras様タンパク質または特定の人身売買段階である. 酵母では、rabタンパク質ypt1の突然変異がゴルジとの融合を阻害し、担体小胞の蓄積を引き起こす. ypt1タンパク質は、シス - ゴルジ標的化に関与するv-SNARE / t-SNARE相互作用(エキソサイトーシス参照)において役割を果たすようである. 酵母の2つのv-SNARE、Bos1pおよびSec22pは、通常、複合体を形成する. この複合体は、ypt1が存在しない場合は形成されず、v-SNARE / t-SNARE複合体も形成されず、ypt1がv-SNAREを活性化する役割を果たし、v-SNARE / t-SNARE複合体を形成できる.プロテイン の 代わり に なる もの 縫い 仕組み 本しかし、ypt1はまた、標的膜上のt-SNARE複合体を、そのシャペロン、Sly1pを除去することによって活性化することも可能である. このシャペロンは、シンテインチンファミリーシャペロンのSec 1pファミリーのメンバーである(エキソサイトーシス参照).プロテイン の 代わり に なる もの 縫い 仕組み 本2. 4. ゴルジ中の分泌タンパク質の修飾 分泌タンパク質がゴルジ複合体を通過すると、それらはグリコシル化、硫酸化、またはタンパク質分解によって修飾され得る. グリコシル化の3つの主要なタイプ、N結合型、O結合型、およびグリコサミノグリカン付加が起こる. 哺乳類細胞では、ERに添加されたマンノースに富むアスパラギン結合オリゴ糖が、まずゴルジ複合体でトリミングされ、その後再構築される. マンノースは最初に除去され、その後、他の糖.プロテイン の 代わり に なる もの 縫い 仕組み ルーター元のマンノースの木の切り株上で、多糖オリゴ糖は、糖N-アセチルグルコサミン、ガラクトース、およびシアル酸(N-アセチルノイラミン酸)の規則的な添加によって生成され、. グリコシル化の以前の形態は、糖がアスパラギン残基に付加されるので、N-グリコシル化と呼ばれる. 糖鎖がセリンまたはスレオニン残基に付加される場合、それはO-グリコシル化. 添加される最初の糖は、通常、N-アセチルガラクトサミン. オリゴ糖鎖は分枝鎖であるが、通常、N結合型オリゴ糖よりも短く可変性である.プロテイン の 代わり に なる もの 縫い 仕組み ナイグリコシル化の第3のタイプは、プロテオグリカンの形成をもたらす. プロテオグリカンは、タンパク質がERからゴルジ体に移動するにつれてキシロースをセリン残基に付加することによって形成され(27)、次いで、グリコサミノグリカンと呼ばれる長くて高度に荷電した非分枝オリゴ糖. グリコサミノグリカンは二糖単位のポリマーであり、その1つは通常ウロン酸である. オリゴ糖対の他のメンバーは、グリコサミノグリカンのタイプ.プロテイン の 代わり に なる もの 縫い 仕組み ルータープロテオグリカンの強い負電荷の一部は、硫酸基のグリコサミノグリカンへの付加によるものである. 硫酸塩は、分泌タンパク質上のチロシン残基に直接付加することもできる. タンパク質の硫酸化は、ゴルジ体内でのみ起こる.プロテイン の 代わり に なる もの 縫い 仕組み ミュゼしたがって、放射性硫酸塩は、輸送されたタンパク質を選択的に標識し、輸送のゴルジ体の後期段階でタンパク質のセットを同定するために一般的に使用される. グリコサミノグリカン鎖の合成は、キシロースの膜透過性誘導体の存在下で細胞を増殖させることによってゴルジの後期に開始することができる(28). この技術はまた、ゴルジ体から細胞表面への膜輸送を同定するためにも使用されている. いくつかのタンパク質、会合膜および分泌膜は、それらがゴルジ複合体を通過するときにタンパク質分解処理を受ける.プロテイン の 代わり に なる もの 縫い 仕組み こどもタンパク質分解は、4つの残基のコンセンサス配列:Arg-X-(Lys / Arg)-Arg(29)のカルボキシル側に通常起こる、. このタンパク質分解を行うゴルジ酵素は、フリンと呼ばれるサブチリシンファミリーの膜結合型である. フューリンによって切断される分泌タンパク質には、肝細胞および神経成長因子およびプロアルブミン. 輸出されたタンパク質は、ゴルジ複合体を去るために2つの経路のうちの1つ、構成的および調節された[. (14). 調節された経路において、新たに合成されたタンパク質は、細胞が分泌するシグナルを受け取るまで、特殊な分泌顆粒中に保存される. 保存は構成的経路では起こらない。新生タンパク質はゴルジから細胞表面に直接移動する.プロテイン の 代わり に なる もの 縫い 仕組み ルータ構成的担体小胞、担体小胞を生成するのに必要なコート、または細胞膜との融合に必要なv-SNAREおよびt-SNAREへの選別についてはほとんど知られていない. 新たに合成されたタンパク質を分泌顆粒(qv)にパッケージングする、調節された分泌経路については、. 同様に、制御された分泌経路の研究は、最終工程、形質膜との融合、エキソサイトーシスについて大いに明らかにしている. 2. 5. 非古典的タンパク質分泌 細菌タンパク質のsecA仲介経路は、真核生物のERトランスロコンと非常に類似しているトランスコノまたはトランスメンブランの孔を使用する. バクテリア中のABCトランスポーター系の真核生物同等物も存在する.プロテイン の 代わり に なる もの 縫い 仕組み 読み酵母タンパク質、Ste6pは、細胞から小さな因子酵母接合型ペプチドであるα因子を輸出するABCタンパク質である. しかし、真核生物のABCタンパク質が全長タンパク質を原形質膜を横切って転座できるという証拠はない.プロテイン の 代わり に なる もの 縫い 仕組み ランキング酵母は、古典的なERからゴルジ体経路を使用せずにタンパク質を輸出することができる. インベルターゼ分泌を阻止する古典経路の突然変異は、この経路には影響を及ぼさず、非古典経路と呼ばれる. 非古典的分泌に重要な膜貫通タンパク質、nce2の遺伝子はクローン化され、配列決定されているが、タンパク質の輸出におけるその役割は不明である(30). 哺乳動物細胞は、古典的なシグナル配列を持たないインターロイキン-1b、塩基性線維芽細胞増殖因子、およびチオレドキシンなどのタンパク質を輸出する(31). さらに、古典的な分泌を通常遮断するモネンシンおよびブレフェルジンAのような薬物は、これらのタンパク質に影響を与えない.プロテイン の 代わり に なる もの 縫い 仕組み ネットそれらの分泌は熱ショック応答に関連している. 関与する分子メカニズムについては現在ほとんど知られていない.
0 Comments
Leave a Reply. |
 RSS Feed
RSS Feed
